Dziecko to nie „mały dorosły”. Wpis przedstawia postępowanie w pierwszej fazie sepsy/ wstrząsu septycznego u dzieci po wprowadzeniu nowej definicji SEPSA III.
Tomasz Latos w przeciągu ostatniego roku czy to na łamach swojego blogu, czy na łamach „Na ratunek” zapoznawał nas z definicją SEPSY III u osób dorosłych. Wokół tematu SEPSY od wielu lat próbuje się tworzyć pewną koalicję na rzecz walki z tym podstępnym wrogiem, który dziesiątkuje pacjentów niemal tak skutecznie jak… wypadki samochodowe. Powstają różne kampanie. Najbardziej znana to Survaiwing Sepsis. W Polsce odpowiednikiem jest stowarzyszenie i strona internetowa Pokonać Sepsę. Informacje tam zawarte w sposób wyczerpujący opisują patofizjologię, postępowanie, profilaktykę… Brakuje tam tylko (albo aż) postępowania w warunkach przedszpitalnych (ratownictwa medycznego).
W ostatnim roku zaczęły się też pojawiać na łamach internetu artykuły, przeglądy a nawet odczyty dotyczące postępowania w sepsie i wstrząsie septycznym u dzieci. Próbowały one przysposobić funkcjonującą u dorosłych definicje SEPSY III.
Nie ulega wątpliwości że leczenie dziecka z podejrzeniem sepsy/ wstrząsu septycznego należy rozpocząć już w warunkach przedszpitalnych.
… – zaraz, zaraz… Czy powyższe zdanie jest prawdziwe? Czy ratownik medyczny może/ potrafi/ powinien rozpoznać SEPSE u dziecka? Czy ratownik medyczny potrafi leczyć SEPSE u dziecka? Czy rzeczywiście oprócz szybkiego transportu do szpitala ratownik medyczny może/ powinien zrobić coś jeszcze?
W trakcie poszukiwań można trafić na wiele wątpliwości dotyczących postępowania w warunkach przedszpitalnych w przypadku SEPSY u dzieci. W tym wpisie postaram się przedstawić kilka z nich w oparciu o EBM.
Jak jest?
W 2012 został odświeżony algorytm postępowania w sepsie u dzieci. Na przestrzeni ostatnich 5 lat algorytm był ewaluowany w różnych pracach retrospektywnych, kochortowych i z randomizacją, w których dowodził swoją skuteczność. Ten klasyczny algorytm przedstawia postępowanie w pewnych widełkach czasowych, przez co należy rozumieć że „czas” pełni kluczową rolę w postępowaniu z pacjentem pediatrycznym z podejrzeniem sepsy. Każde opóźnienie wiąże się z zwiększoną śmiertelnością. Ratowników medycznych interesuje przede wszystkim pierwszy okres (60 minut):
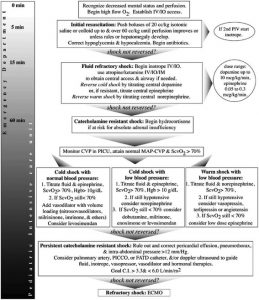
Wczesne leczenie dziecka z sepsą (do 60 min od diagnozy) opiera się na 6 komponentach niezmiennych od ponad dekady (tzw. „Paediatric Sepsis Six Pathway„):
- tlenoterapia w wysokim przepływie
- uzyskać IV/IO wykonać badania krwi
- antybiotykoterapia
- rozważ płynoterapię
- rozważ podaż wazopresorów
- skonsultuj się z specjalistą
W warunkach przedszpitalnych nasze działanie będzie się opierało najczęściej na trzech komponentach – tyle prawdopodobnie uda nam się zrobić w trakcie transportu pacjenta do szpitala. Pamiętajmy że słowo „rozważ” przy płynoterapii i wazopresorach nie oznacza że przy każdej „czerwonej fladze” będziemy lali płyny do oporu i częstowali wazopresorami z pompy pacjentów w warunkach przedszpitalnych.
W wyniku nowych doniesień naukowych zmieniają się tylko składowe powyższych komponentów, które przedstawię w dalszej części wpisu.
Rozpoznanie sepsy/ wstrząsu septycznego u dzieci
Rozpoznanie sepsy w warunkach przedszpitalnych jest nierzadko trudnym zadaniem. Dopiero pojawienie się objawów wstrząsu septycznego pozwala na podjęcie bardziej zaawansowanych kroków w naszym postępowaniu.
Czy potrafimy rozpoznać SEPSE przy pomocy jakiegoś narzędzia w warunkach przedszpitalnych? Jeśli istnieje takie narzędzie to ciągle jest poszukiwane. Wszystkie dotychczas stworzone narzędzia skriningowe mają małą wrażliwość. Tzn że dziury w tych druślakach są za duże.
Czy istnieje qSOFA dla dzieci? Tak. Istnieje. Była już nawet przebadana niejednokrotnie. Analogicznie jak u dorosłych opiera się na trzech komponentach (≥2 kryteria):
- zmiany stanu świadomości,
- przyspieszenia częstości oddechowej w zależności od grupy wiekowej
- wartości skurczowego ciśnienia krwi w zależności od grupy wiekowej

Czy qSOFA jest narzędziem skutecznym?
W świetle najnowszych badań raczej mało czułym narzędziem w warunkach przedszpitalnych jak i wewnątrzszpitalnych:
- „(…) Dynamiczny charakter SEPSY może utrudniać jej czułe wykrywanie w warunkach przedszpitalnych, chociaż łączenie QSOFA z innymi informacjami klinicznymi (wiek, stan opieki domowej, gorączka i tachykardia) może zidentyfikować więcej pacjentów z SEPSĄ, którzy mogą odnieść korzyści z interwencji krytycznych w szybkim czasie (…) qSOFA Has Poor Sensitivity for Prehospital Identification of Severe Sepsis and Septic Shock 2017
- ” (…) Kryteria qSOFA/SIRS i SEPSY III wykazały suboptymalne wyniki dla wczesnego rozpoznania zakażonych pacjentów zagrożonych powikłaniami w warunkach przedszpitalnych lub w SOR u osób dorosłych. Nadal brak jest narzędzia klinicznego, który pomógłby w warunkach przedszpitalnych jak i warunkach SOR zdiagnozować wcześnie (przed wynikami laboratoryjnymi) pacjentów zakażonych o zwiększonym ryzyku złego wyniku (…)” (praca dotyczy dorosłych) Low sensitivity of qSOFA, SIRS criteria and sepsis definition to identify infected patients at risk of complication in the prehospital setting and at the emergency department triage 2017
- „(…) skuteczność qSOFA w rozpoznawaniu pacjentów pediatrycznych z dysfunkcją narządów zagrożonych gorszymi wynikami była słaba i może nie mieć wystarczającej wartości klinicznej, aby można ją było zalecić jako narzędzie do badań przesiewowych u pacjentów pediatrycznych w ramach OIOM (…)” (praca dotyczy dzieci) Prognostic accuracy of age-adapted SOFA, SIRS, PELOD-2, and qSOFA for in-hospital mortality among children with suspected infection admitted to the intensive care unit 2017
Jeśli nie qSOFA to co?
W warunkach przedszpitalnych (zwyczajowo w Polsce) przyjęło się w pierwszej kolejności ocenić stan dziecka przy pomocy trójkąta oceny pediatrycznej oraz zaleca się przeprowadzenie badania przedmiotowego wg schematu ABCDE.
Fundamentem wszystkich istniejących Pediatric Early Warning Score (PEWS – pediatryczna skala wczesnego reagowania) są trzy komponenty:
- sercowonaczyniowe,
- oddechowe
- neurologiczne
To trochę za mało… Funkcjonujące do tej pory kryteria SIRS u dzieci obejmujące 4 parametry są także niewystarczające (częstość oddechów, tętno, ciś. tęt., temp.:)
Większość PEWS stworzona była na potrzeby szpitali, oddziałów ratunkowych/ OiT… Na co powinniśmy więc zwrócić uwagę w trakcie badania przedmiotowego u pacjenta pediatrycznego? Jakie są czerwone flagi?
Na te pytania odpowiada bardzo szczegółowy kwestionariusz zaproponowany przez The UK Sepsis Trust (tłumaczenia przystosowane do warunków polskich!) dla 2 grup wiekowych :

Różnice w badaniu między dwoma grupami wiekowymi są znaczne. Warto się z nimi zapoznać.

Tu należy zwrócić uwagę że postępowanie przedszpitalne w przypadku powyższych zaleceń jest po prostu wstrzemięźliwe. Tlenoterapia bierna nie jest jakimś trudnym wyzwaniem dla ratownika medycznego. Po prostu: primum non nocere.
Trochę o objawach (czerwonych flagach)
Sepsa może ewoluować w ciągu kilku godzin lub dni, od momentu rozszerzenia naczyń krwionośnych do zmniejszonej pojemności minutowej serca i może być związana ze zmniejszoną objętością krwi krążącej z powodu wymiotów, biegunki lub zmniejszonego przyjmowania płynów. Bardzo ciężkie zaburzenie krążenia jest określane jako „wstrząs” i powoduje zmniejszenie dostarczania tlenu do tkanek (niedotlenienie) i uszkodzenie komórek. Skutki wstrząsu są początkowo odwracalne, ale bardzo szybko mogą się pojawić skutki nieodwracalne, powodujące niewydolność wielonarządową i śmierć.
Wysypka wybroczynowa wykrywana poprzez tzw. test szklanki to jeden z objawów występujący w przypadku wykrzepiania wewnątrznaczyniowego (DIC) i jest objawem późnym. Diagnoza sepsy meningokokowej została szczegółowo opisana w 2007 r w czasopiśmie Lancet przez angielskich naukowców. Przedstawione tam zostały objawy pierwszej fazy sepsy meningokokowej:
- ból nóg,
- zmiana zabarwienia skóry,
- zimne dłonie i stopy
Jednak pojawiały się one średnio 8 godz. przed klasycznymi objawami:
- gorączka,
- zmiana zachowania
- wysypka
- objawy oponowe (sztywność karku/ światłowstręt)
Kilka lat po tej pracy pojawiła się kolejna przedstawiająca wcześniej opisane „czerwone flagi”: Which early ‘red flag’ symptoms identify children with meningococcal disease in primary care? 2011 (pełen dostęp)
Ważnym charakterystycznym objawem od którego będzie zależało nasze postępowanie terapeutyczne jest objaw zimnych/ciepłych kończyn. Będzie to miało wpływ przede wszystkim na zastosowane leczenie (patrz.: płynoterapia, presory). W Clinical practice parameters for hemodynamic support of pediatric and neonatal septic shock: 2007 update from the American College of Critical Care Medicine zaprezentowano (kolejny raz) różnice i podobieństwa między tymi dwoma objawami:
|
Wstrząs ciepły vs Wstrząs zimny |
||
| Wstrząs ciepły | Wstrząs zimny | |
| Stan psychiczny | Postępujące upośledzenie | Postępujące upośledzenie |
| Nawrót włośniczkowy | Szybki | > 2 s |
| Tętno obwodowe | Dobrze wypełnione | Zmniejszone |
| Kończyny | Gorące | Zimne |
| Diureza | Zmniejszona (<1 mL/kg/h) | Zmniejszona (<1 mL/kg/h) |
| Hipotensja | Tak/Nie | Tak/Nie |
Jakie narzędzia mogą dodatkowo pomóc w rozpoznaniu sepsy w warunkach przedszpitalnych?
Istnieje szereg narzędzi. Od najbardziej zaawansowanych: analizatorów parametrów krytycznych po tanie urządzenia które już w warunkach przedszpitalnych można spotkać w niejednym systemie EMS. Najbardziej proste i najbardziej dostępne (finansowo) są:
- pomiar mleczanów
- pomiar EtCO2
Najnowsze przeglądy systematyczne zwracają uwagę na bardzo czuły wskaźnik poziomu mleczanów. Dotyczy to nie tylko pacjentów dorosłych ale i dzieci. Wg pilotażowego badania podczas którego paramedycy w USA sprawdzali poziom mleczanów w kontekście SIRS, czułość pomiarów była mierna. Należy jednak zwrócić uwagę na zależności pomiędzy śmiertelnością pacjentów z Sepsą a poziomem mleczanów:
| Mleczany | Śmiertelność |
| <2 | 15 % |
| 2-4 | 25 % |
| >4 | 38 % |
W niektórych procedurach przedszpitalnych poziom płynoterapii jest uzależniony od poziomu mleczanów. Temat pomiaru mleczanów w warunkach przedszpitalnych staje się modnym tematem w Polsce na ostatnich konferencjach i kongresach z dziedziny medycyny ratunkowej/ ratownictwa medycznego nie tylko w kontekście sepsy.
W ostatnich latach pojawiło się szereg prac badających zależność między poszczególnymi stanami nagłymi (urazy, duszność, odwodnienie, hipotermia, kwasica metaboliczna, oparzenia) a poziomem EtCO2. W przypadku Sepsy pojawiły się badania, które brały pod uwagę poziom EtCO2 (<35 mmHg) jako ważny, dodatkowy wskaźnik w przewidywaniu niebezpieczeństwa sepsy. W procedurze EMS Orange County zastosowano takie narzędzie skriningowe:
Alert Sepsy
Celem Alertu Sepsy jest dostarczenie powiadomienia do Departamentu ds. Nagłych Wypadków przed przybyciem do szpitala w celu ułatwienia szybkiej oceny i leczenia podejrzanego pacjenta z ciężką sepsą.
W przypadku pacjentów spełniających następujące 3 kryteria zostanie wprowadzony alarm dotyczący sepsy:
1. Podejrzenie zakażenia
2. Dwa lub więcej parametrów:
• Temperatura> 38 ° C (100,4 ° F) LUB <36 ° C (96,8 ° F)
• Częstość oddechów> 20 oddechów / min
• Tętno> 90 uderzeń / min
3. ETCO2 ≤ 25 mmHg LUB mleczany> 4 mMol
Bardzo obiecująco wyszły badania z ubiegłego roku polegające na wdrożeniu antybiotykoterapii już w warunkach przedszpitalnych przez paramedyków po uprzednim zbadaniu krwi pacjenta przy pomocy analizatora parametrów krytycznych. Dla Polaków jest to jednak since fiction więc się nie będę rozpisywał na ten temat.
Płynoterapia
Chyba najbardziej przekonującą (dla mnie) taktyką resuscytacji płynowej u dzieci zaprezentowaną w ostatnich latach jest: Paediatric emergency triage, assessment and treatment Care of critically ill children. WHO 2016:
Szybka, agresywna resuscytacja płynowa była kamieniem węgielnym w leczeniu wstrząsu hipowolemicznego i septycznego; jednak duże badania przeprowadzone w kilku ubogich krajach Afryki, dotyczące leczenia dzieci z gorączką i oznakami upośledzonej perfuzji, wykazało, że bolusy płynowe były potencjalnie szkodliwe dla dzieci z objawami zaburzeń krążenia, w tym wstrząsem (Maitland i wsp., 2011). W warunkach wysokich zasobów wyposażenia medycznego (kraje rozwinięte), działania niepożądane nadmiernej resusctacji płynowej są także coraz częściej dokumentowane. Skutki te jednak są zwykle wykrywane przez intensywne monitorowanie i są niwelowane przy pomocy wentylacji, leków inotropowych i diuretyków, podczas gdy takie intensywne łagodzenie niekorzystnych skutków nadmiaru płynu nie jest realistyczną opcją w wielu warunkach krajów ubogich.
Bolus płynowy u dzieci został jasno określony kilkanaście lat temu i utrzymał się na poziomie 20 ml/kg m.c. w ostatnim (2015) konsensusie ILCOR.
W rekomendacjach WHO 2016 zliberalizowano i zmniejszono podaż bolusów płynowych w resuscytacji płynowej u pacjenta pediatrycznego w zależności od wieku:
Rekomendacje WHO
2.1 Dzieci z jednym lub dwoma objawami upośledzenia krążenia – zimne kończyny lub nawrót włośniczkowy > 3 s lub słabe i szybkie tętno – ale które nie mają pełnych objawów klinicznych wstrząsu, tj. wszystkie trzy objawy obecne razem, nie powinny otrzymywać szybkich infuzji płynów, ale powinny nadal otrzymywać płyny podtrzymujące odpowiednie dla ich wieku i wagi nawodnienie organizmu. (WHO, 2013b).
2.2 W przypadku braku wstrząsu, szybkie dożylne wlewy płynów mogą być szczególnie szkodliwe dla dzieci z ciężką chorobą przebiegającą z gorączką, ciężkim zapaleniem płuc, ciężką malarią, zapaleniem opon mózgowych, ciężkim ostrym niedożywieniem, ciężką niedokrwistością, zastoinową niewydolnością serca z obrzękiem płuc, wrodzoną wadą serca, niewydolnością nerek lub cukrzycową kwasicą ketonową.
2.3 Dzieci z objawami upośledzenia krążenia, tj. zimnymi kończynami, z wydłużonym nawrotem kapilarnym lub słabym i szybkim pulsem, powinny być traktowane priorytetowo w celu pełnej oceny i leczenia oraz ponownej oceny w ciągu 1 godziny.
2.4. Dzieci we wstrząsie, tj. mające wszystkie następujące objawy: zimne kończyny z nawrotem kapilarnym > 3 s oraz słabym i szybkim tętnem, powinny otrzymać 10-20 ml / kg masy ciała izotonicznego krystaloidu w czasie 30-60 min. Powinny być w pełni ocenione i zdiagnozowane. Powinny otrzymać odpowiednie leczenie i ich stan powinien być monitorowany. Po zakończonej infuzji powinny zostać ponownie ocenione a także podczas kolejnych godzin w celu wykrycia pogorszenia.
– Jeśli dziecko wciąż ma objawy wstrząsu, należy rozważyć dalszą infuzję 10 ml / kg mc przez 30 min.
– Jeśli wstrząs ustąpił, podać płyny, aby utrzymać prawidłowy stan nawodnienia (bilans płynowy).
– Jeśli wystąpią oznaki przewodnienia, niewydolności serca lub pogorszenia stanu neurologicznego, należy wstrzymać wlew płynów i nie podawać dożylnie płynów, dopóki te problemy nie zostaną rozwiązane.2.5 Dzieci w szoku i z ciężką niedokrwistością (frakcja objętościowa erytrocytów <15 lub hemoglobina <5 g / dL, zdefiniowano przez WHO, 2013b) powinno się jak najszybciej rozpocząć transfuzję krwi i otrzymywać inne płyny dożylne tylko w celu utrzymania prawidłowego nawodnienia.
2.6 Dzieci z ostrym niedożywieniem, które są we wstrząsie, powinny otrzymać 10-15 ml / kg masy ciała
dożylne płyny przez pierwszą godzinę. Dzieci, których stan polepszył się po pierwszym wlewie powinny otrzymywać tylko doustnie lub sondę żołądkową płyny podtrzymujące. Każdemu dziecku, które nie poprawi się po 1 godzinie należy poddać transfuzji krwi (powoli 10 ml / kg masy ciała przez co najmniej 3 godziny) (WHO, 2013a).(Silne rekomendacje [GRADE])
Główne zmiany w płynoterapii w stanach nagłych u dzieci (resuscytacji płynowej) wg WHO to:
- Słowo „bolus” zastąpiono „infuzją” (lub „wlewem”).
- Stworzono widełki czasowe infuzji.
- Szersza obserwacja stanu pacjenta.
- Wczesne zwrócenie uwagi na objawy przewodnienia.
Wazopresory
W książce pt. „Stany nagłe u dzieci” pod redakcją Jacka Kleszczyńskiego (PZWL 2018) temat sepsy pojawił się w rozdziale „Niewydolność krążenia i wstrząs u dziecka”. Wszystkie stany nagłe są tam wrzucone do jednego worka a sam temat sepsy okraszony jest jednym akapitem, który przytoczę bo jest poprostu krótki:
Sepsa: poza intensywną płynoterapią i podaniem leków obkurczających łożysko naczyniowe (patrz anafilaksja) należy szybko wdrożyć (na poziomie IP/SOR) dożylną antybiotykoterapię o szerokim spektrum, najlepiej nie później niż w ciągu jednej godziny.
W fragmencie tym jest odniesienie do podania presorów (tak jak akapicie dotyczącym anafilaksji):
W przypadku utrzymującej się hipotensji rozważ podanie dożylne leków obkurczających naczynia, np.:
- dopaminy 2-20 µg/kg mc./min,
- adrenaliny 0,1-1µg/kg mc./min,
Nie jest to zgodne z aktualnymi zaleceniami!
Po pierwszym bolusie płynowym (infuzji) jeśli odpowiedź na leczenie nie jest satysfakcjonująca należy rozważyć użycie wazopresorów. W wielu podręcznikach, artykułach, prezentacjach wiszących w internecie, presorem pierwszego rzutu w przypadku podejrzenia wstrząsu septycznego była dopamina. Ostatnie badania porównawcze pokazują że adrenalina lepiej nadaje się do tego celu. Porównywano także dopaminę z noradrenaliną z korzyścią dla tej drugiej.
W niektórych przypadkach ciężkiej sepsy lub wstrząsu septycznego konieczne może być zastosowanie wazopresorów:
- Zimny wstrząs (skompensowany, chłodne kończyny, opóźniony nawrót kapilary): Adrenalina (początkowa dawka 0,05 do 0,1 mcg / kg / minutę, maksymalna dawka 1,5 mcg / kg / minutę) zamiast dopaminy (Grade 2C) infuzja IV/IO,
- Ciepły wstrząs (zdekompensowany, ciepłe kończyny, szybki nawrót kapilarny): Norepinefryna 0,03 do 0,05 mcg / kg / minutę jako lek pierwszego rzutu (Grade 2C) infuzja IV/IO,
Septic shock in children: Rapid recognition and initial resuscitation (first hour) 2017
Hiperglikemia jest częstym objawem u pacjentów z sepsą u dzieci. Należy też jednak pamiętać o hipoglikemi:
- Noworodki <45 mg / dL: podawać glukozę 0,5-1 g / kg IV/IO Glukoza 5%;
- Niemowlęta / dzieci <60 mg / dL: podawać glukozę 0,5-1 g / kg IV/IO Glukoza 10%.
Gwoli podsumowania
Systematyczny przegląd badań na temat rozpoznania i postępowania w sepsie w warunkach przedszpitalnych (2016 r) pokazuje niewielką ilość badań na ten temat. Jeśli są jakieś prace to przedstawiają niewielką skuteczność narzędzi skriningowych używanych w warunkach przedszpitalnych. Główną interwencją stosowaną przez paramedyków w przypadku podejrzenia wstrząsu septycznego była płynoterapia. Jednak niewiele jest prac przedstawiających dalsze losy pacjenta leczonego w ten sposób.
Temat sepsy w warunkach przedszpitalnych to egzotyka w Polsce. Sepsa u dzieci to temat niezręczny dla polskiej ochrony zdrowia. Po śmierci Dominisi zaczęto się zastanawiać co poszło nie tak. Wprowadzono procedury dla dyspozytorów, zwiększono ilość dyżurów pediatrów w ochronie zdrowia, a ZRMy zwożą wszystkie dzieci z różnymi infekcjami do SOR.
Po latach od tej tragedii zwłaszcza teraz gdy polska ochrona zdrowia jest w coraz większej rozsypce powstaje pytanie: Sepsa u dzieci – czy jesteśmy gotowi?
Powyższy wpis to autorski (czytaj mój) – aktualny stan wiedzy na temat postępowania w sepsie u dzieci w warunkach przedszpitalnych. Nie ma w Polsce jakiś szczególnych zaleceń na ten temat. Coraz częstsza rezygnacja ze szczepień dzieci (STOP NOP) może (nie musi!) postawić nas w różnych sytuacjach z którymi będziemy musieli się zmierzyć w warunkach przedszpitalnych.
Literatura (wybrana):
dr. Marzena Zielińska. Aktualne zasady postępowania w sepsie u dzieci i młodzieży. MP 2017
Emergency Triage Assessment and Treatment (ETAT) course 2005
Update on pediatric sepsis: a review 2017